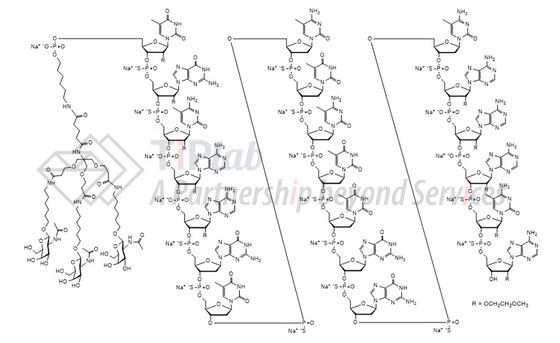
Donidalorsen 是一种ASO-GalNAc缀合物,包括靶向前激肽释放酶(PKK,激肽释放酶的前酶)的反义寡核苷酸 (ASO),共价连接至含有三个GalNAc 残基的配体,以促进 ASO 递送至肝细胞。其中,ASO部分是典型的 gapmer 结构,即包括 2′-O-MOE 修饰的核苷酸侧翼(wings)和中心DNA 间隔区域(gap)。
Donidalorsen通过与PKK mRNA结合,引起核糖核酸酶H1 (RNase H1)介导的PKK mRNA降解,从而导致PKK蛋白生成减少。在HAE患者中,C1抑制剂(C1-INH)的缺乏或功能障碍会导致血浆激肽释放酶活性过高、缓激肽生成和血管性水肿发作。Donidalorsen可降低PKK浓度,从而防止HAE患者缓激肽过量生成。
HAE 是一种罕见遗传性疾病,会导致身体各个部位反复出现严重肿胀(血管性水肿)。据估计,美国约有 7,000 人患有 HAE。目前已有多款药物获批用于治疗或预防HAE,药物类型包括抗体、小分子、多肽类药物等。另外,Intellia治疗HAE的 CRISPR 体内基因编辑疗法Lonvo-z(Lonvoguran ziclumeran)处于临床3期阶段。
Dawnzera 的获批基于一项 3 期OASIS-HAE 研究的积极结果。该研究达到了其主要终点:Dawnzera Q4W 在 24 周内显著降低了每月 HAE 发作率,与安慰剂相比降低了 81%。
围绕donidalorsen的方法专利家族PCT/US2012/041743和活性成分专利家族PCT/US2015/028765的保护期将在2032和2035年。
方法专利家族:已在美国和欧洲获得授权,保护范围比较宽泛,涉及使用与 KLKB1 核酸至少 90% 互补的修饰寡核苷酸预防性治疗HAE的方法。
活性成分专利家族:已在中美欧日等获得授权,权利要求涉及一类分子或具体分子结构。比如,限定donidalorsen的碱基序列和缀合物或者限定缀合物的具体结构式。
另外,Ionis还拥有涉及调节PKK表达的ASO的专利家族,比如:2014年递交的PCT/US2014/053266涉及一种经修饰的寡核苷酸,涵盖多种核碱基序列,也包括donidalorsen的ASO序列。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
