Del-desiran 是一款在研药物,旨在针对 DM1 的潜在遗传病因。目前尚无针对 DM1 患者的获批药物。Del-desiran 已获得 FDA 的突破性疗法认定、孤儿药认定和快速通道认定,以及 EMA 的孤儿药认定。Del-desiran 也是日本首个获得孤儿药认定的 DM1 在研药物。
在启动 HARBOR 试验之前,Avidity 已与包括 FDA 在内的全球监管机构就 del-desiran 的注册流程进行了协调。公司计划从 2026 年下半年开始在美国 、欧盟和日本等地提交上市申请。
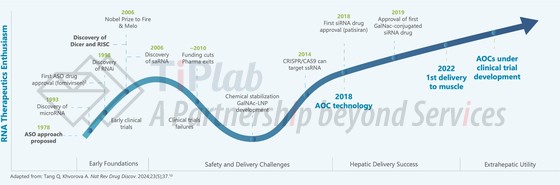
Avidity Biosciences 致力于提供新型 RNA 疗法—抗体寡核苷酸偶联物(AOC),首次在临床试验中成功通过全身给药将 RNA 靶向递送至肌肉。其AOC平台包括靶向转铁蛋白受体 1(TfR1,在肌肉细胞中高度表达)的单抗通过接头与一个或多个 siRNA 或 PMO 结合而成,旨在将 RNA 疗法递送至肌肉。
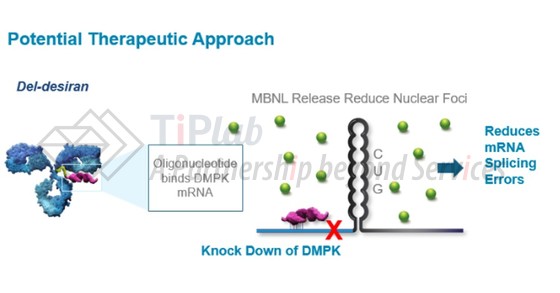
强直性肌营养不良症 1 型 (DM1) 是一种罕见的遗传性(常染色体显性)进行性神经肌肉疾病,该疾病因 DMPK 基因中 CUG 三联体重复序列数量增加引起的。具体而言,突变的 DMPK mRNA 会与关键的 CUG 结合蛋白 MBNL 结合,阻止 MBNL 处理许多其他基因 mRNA 的正常功能。
Del-desiran 是 Avidity 公司利用其 AOC 平台开发而成,由靶向 TfR1 的单抗与靶向 DMPK mRNA 的siRNA 结合而成,能够通过降低 DMPK mRNA 水平、释放 MBNL来解决疾病的根本病因。
与del-desiran相关专利家族 PCT/US2018/064359 涉及核苷酸缀合物,目前有多个授权和在审成员,保护主题涵盖活性成分和适应症等,范围既有宽泛又有具体,比如:US10881743B2限定siRNA缀合物的结构组成,包含抗转铁蛋白受体抗体(两个VH和两个VL)和靶向 DMPK mRNA 的siRNA分子。US11253607B2则涉及ASO缀合物。US11246941B2涉及治疗方法。CN111902148B限定siRNA缀合物中siRNA的可选序列组合。
据 Avidity 披露,截至2024年12月,其共有29个专利家族涉及AOC平台,涵盖AOC缀合物的结构、寡核苷酸化学结构及其序列和抗体等,预计到期日在 2037 年至 2045 年之间。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
