前面我们提到,目前蛋白降解双功能分子领域内玩家们的创新主要集中在结合治疗靶点的“弹头”和蛋白降解效应物配体两个部分。对于在这两个部分进行创新的玩家,在考虑专利策略时的侧重点会有所不同。其中对于在“弹头”上进行创新的玩家而言,通常基于PROTAC这一已完成初步验证的形式开发新的分子,其创新会较多地参考现有的分子片段,关于这些现有的分子片段是否存在相应的专利障碍,是这部分玩家主要考虑的专利问题。而在专利申请上一般围绕其核心的产品分子保护其具体结构或通式,这部分的申请策略是相对明确的。
整体上来说,对于这类玩家而言所需考虑的专利风险是比较复杂且分散的。蛋白降解双功能分子包括效应物配体、“弹头”部分和Linker三个元件,单独的每个部分及其组合均有可能引入专利风险。结合各部分的功能,效应物配体和“弹头”部分的风险更加复杂且棘手,而Linker部分及其组合方面的风险则相对简单并容易解决。
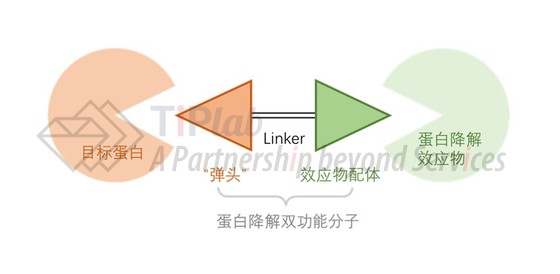
具体来说,对于效应物配体部分,其决定了目标蛋白将通过何种方式被降解,可能存在效应物用于双功能分子以及效应物配体分子结构的专利风险,侧重在“弹头”部分进行创新的玩家在效应物配体的选择可能主要基于现有验证过的技术,因此,其风险情况主要取决于这些现存技术的风险水平并针对性进行规避设计。
对于“弹头”部分,其决定了降解的目标蛋白即“治疗靶点”,风险可能来自于“治疗靶点”以及“弹头”部分的分子结构。侧重在“弹头”部分进行创新的玩家需要提前掌握现有技术的风险并设计具有一定创新度的结构,以实现规避已有风险并同时进行专利保护。
对于Linker部分,其作用主要是用来连接效应物配体和“弹头”部分,相对重要性不及上述两个部分,创新高度有限,决定了其风险相对更低。
对于不同部分的组合,通常专利保护出现比较晚且范围会比较具体,比如,会限定至具体的分子结构,所以其风险也相对容易解决。
接下来,我们来展开分析下各部分风险的情况及其可能的解决方式。
蛋白降解效应物及其配体的专利风险
正如前面提到的,在效应物配体部分可能存在效应物用于双功能分子以及效应物配体分子结构的专利风险。
将具有降解功能效应物用于设计双功能分子的相关专利的申请日比较早,被认为是领域内的底层专利。这类专利的主要发明点在于双功能分子的作用原理,不会限定到具体的治疗靶点和效应物配体的分子结构,因此,如果利用的原理相同,则很难通过改变具体的配体分子结构进行规避,作用原理层面的专利往往是领域内玩家首先需要关注的风险来源。
对于通过“弹头”创新设计新型PROTAC分子的玩家,其机理专利即为通过招募E3连接酶来降解治疗靶点的相关专利。早在1999年2月,Proteinex就已递交并获得了授权专利US6306663B1,其保护产生用于激活靶蛋白泛素化的化合物的方法,该化合物含有共价连接的两个结合部分,分别结合泛素化识别元件和目标蛋白。

基于对两个元件的功能限定,PROTAC中E3泛素连接酶配体即属于泛素化识别元件,“弹头”部分即为靶蛋白结合元件,因此只要是产生PROTAC分子,即落入了该专利的保护范围。不过,目前该专利家族的成员均已到期,当下可以不用担心该专利家族所带来的专利风险。
对于效应物配体分子结构层面的风险,在“弹头”上进行创新的玩家倾向于现有的已经过验证的分子,比如最常见的CRBN配体。当筛选合适的CRBN配体时,需要关注是否存在相应结构通式及具体分子的专利风险。基于我们的了解,关于CRBN配体结构授权且仍有效的专利,其母核结构各具特色,或者是与特定的Linker或/和“弹头”结构组合进行保护,我们认为是存在一定的规避设计空间的。
例如,Kymera设计的一类CRBN配体(US11485743B2),它保护的母核结构有一个明显的特点是存在一个含硫连接子,相较于上市的三款度胺类药物的结构差异比较显著。
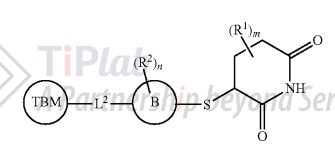
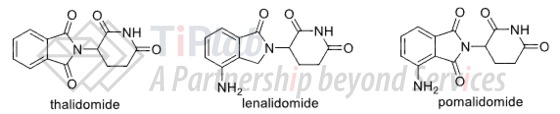
由于“弹头”创新的玩家重点不在于CRBN配体的效果上是否还能更进一步,此外考虑到CRBN配体的选择比较多样化,因此,对于上述这类专利,关键是在项目早期就掌握不同母核结构的专利保护范围,以便后续分子结构设计时能更好地规避相应的风险。例如,目前有许多常见的CRBN配体母核结构并不涉及该含硫连接子,可以考虑选择这类母核结构规避该专利所带来的风险。
“弹头”部分的专利风险
相较于效应物配体部分,若采用常用的CRBN配体时,其主要的风险来源于CRBN配体的分子结构,而“弹头”部分的选择作为该类玩家创新的关键,所需要考虑的风险来源更为复杂。
首先,在“治疗靶点”方面不仅需要考虑蛋白降解双功能分子用于靶向特定治疗靶点的风险,还需要考虑涉及“治疗靶点”和疾病关系的专利风险。其次,由于“弹头”结构设计通常会基于现有分子片段进行改造,同样需要考虑因此引入的专利风险。
治疗靶点相关的专利风险是立项早期就需要重点关注的风险来源,因为这类专利往往不会限定相应的分子结构,当我们使用的靶点或/和适应症相同时,一般很难通过分子结构的改造绕开权利要求的保护范围。若企业在立项早期阶段就能掌握这类专利风险,可以在靶点或/和适应症的选择时提前进行规避。此外,由于不同国家/地域的专利审查尺度不同,即使是相同的技术方案,其专利授权的范围也不尽相同,企业也可以合理规划未来的商业化策略进行规避。
针对靶点相关的专利风险,一方面需要考虑涉及治疗靶点和疾病关系的专利,这类专利本身可能与蛋白降解双功能分子领域并不相关,是比较容易被忽略的一类风险专利。如:CN107257691B,权利要求29保护了抑制EGFR家族成员信号传导的试剂在制备用于治疗低级别浆液性卵巢癌的药物中的用途。

虽然该专利并不涉及蛋白降解双功能分子,但我们理解靶向EGFR的蛋白降解双功能分子同样也可能具备抑制EGFR家族成员信号传导的功能,若未来产品的适应症涉及低级别浆液性卵巢癌,就有可能落入该权利要求的字面范围内。由于该专利在欧洲和美国并未获得不限抑制剂类型的宽泛专利保护,未来可以考虑通过适应症的选择或者调整商业化节奏来进行规避。
另一方面,还需要考虑宽泛保护靶向特定降解靶点的双功能分子的专利风险。例如:Craig Crews递交的US10946017B2,权利要求1宽泛保护了靶向TBK1的PROTAC分子,PROTAC分子的三个组成部分未作任何结构限定,基本很难通过结构改造来进行规避设计,不过可以考虑从商业化地域和时间上进行风险规避。

除了靶点相关的专利风险外,这类玩家通常会以已获得临床验证或商业化的小分子抑制剂作为先导化合物进行结构改造来设计“弹头”,随着这类小分子在临床上或商业上获得成功,会有不同的主体针对该抑制剂结构进行改造并申请专利。此外,对于将特定小分子抑制剂首次设计成蛋白降解双功能分子的玩家,不排除可能他们会拥有宽泛保护“弹头”为该小分子抑制剂的蛋白降解双功能分子,但不限定Linker和效应物配体结构的专利。所以需要全面地排查“弹头”结构相关的专利风险,而不局限于来自原研主体的专利风险。
Linker及分子组合的专利风险
考虑到Linker往往与靶点配体和效应物配体密切相关,我们认为仅限定Linker的结构,对于“弹头”部分和效应物配体部分不进行任何结构限定的权利要求授权难度较大,往往需要与“弹头”部分或/和效应物配体部分的结构组合限定来进行保护。而且Linker的可替代性较强,未来即使存在相关专利风险,也可以通过简单的结构改造来进行规避。所以,Linker的专利风险相对于前两个组成部分,会相对可控一些。考虑到Linker结构和连接位点的确定后,整体分子结构也基本确定了,我们建议可以在后续排查整体分子结构的同时,一并排查Linker层面的专利风险。
提到整体分子结构的风险排查,我们这里想强调一下,专利风险排查过程是动态调整和循序渐进的。随着研发进展的不断推进,双功能分子的结构特征越来越明确,不同元件可能还伴随着结构优化,那么待分子结构基本确定时,仍需对整体的产品分子进行补充风险排查,以排除来自蛋白降解双功能分子组成部分的两两组合的结构通式或整个分子结构通式的专利风险。此外,对于存在结构优化的部分,可能还需要对该部分元件单独进行补充分析。
结语
总的来说,对于“弹头”创新设计新型PROTAC分子的玩家而言,由于PROTAC的底层机理专利障碍目前已消失,管控专利风险的关键在于梳理清楚不同元件或其组合的风险点来源,并根据研发进展依次推进相应的风险排查。具体而言,在早期立项确定治疗靶点和适应症时就需要首先关注弹头部分中“治疗靶点”相关的专利风险,因为这部分风险很难通过后期具体分子结构的优化来进行规避。与此同时,我们也可以尽早关注“弹头”部分和效应物配体部分的相关专利,并与研发配合对母核结构进行设计,使其能够规避现有风险并同时满足可专利性。而Linker部分的风险,我们认为相对比较可控,可以在整体分子基本确定后,与整体分子的专利风险一并排查。
