Vigil 成立于2020年,专注于开发神经退行性疾病的新型疗法来恢复小胶质细胞(大脑免疫系统的哨兵细胞)的警惕性。
今年5月份,赛诺菲宣布以4.7亿美元收购 Vigil,并在6月份对 Vigil 进行了 4000 万美元的战略投资,其中包括对 VG-3927 的独家许可、授权或权利转让的优先谈判权,以用于该产品的研究、开发、生产和商业化。
Vigil 最初由 Amgen 参与成立,其技术和早期候选药物源自 Amgen 的研发项目,包括TREM2 相关的单抗和小分子项目。
在本次收购中,不包括 Vigil 的一款 TREM2 激动型单抗 VGL101(后称 iluzanebart),该抗体的 2 期研究未能达到疗效终点,已经返还给Amgen。
小胶质细胞对于维持正常的大脑健康至关重要。它们持续感知并响应损伤指标,例如感染、细胞碎片或斑块积聚,这些指标可通过 TREM2 受体检测到,从而将小胶质细胞转化为神经保护状态。
TREM2 是一种在小胶质细胞上特异性表达的跨膜受体。功能性 TREM2 是脑损伤配体的受体,当 TREM2 功能丧失时,小胶质细胞就无法转化为神经保护状态,从而导致碎片堆积,最终导致神经退行性病变。TREM2 信号通过一个协同信号复合物传递,该复合物包含胞内蛋白 DAP12、SYK和 SRC。
已有研究证明了 TREM2 在预防神经退行性疾病中发挥的关键作用,TREM2 基因突变是阿尔茨海默病的最大风险因素之一。这构成了通过治疗激活 TREM2 信号传导来治疗神经退行性疾病的理论基础。
已有数据显示 TREM2 变体 (R47H) 中的特定突变是阿尔茨海默病(AD)的遗传风险因素之一,近期研究还显示 TREM2 表达增加对 AD 具有保护作用。通过使用激动剂激活 TREM2,增强小胶质细胞在 AD 中的天然神经保护功能。
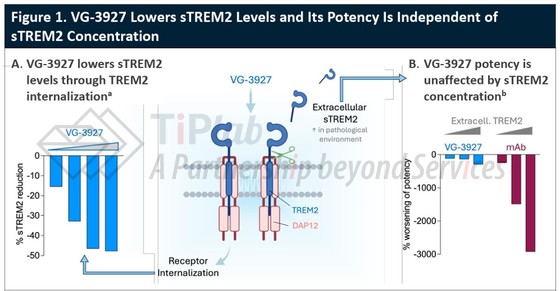
VG-3927 会导致 TREM2 复合物内化,从而保护 TREM2 的胞外结构域免于裂解,并降低可溶性 TREM (sTREM2) 水平。与单抗相比,小分子 TREM2 激动剂具有更广泛的给药选择和更优异的脑渗透性。
Vigil有多个家族涉及作为 TREM2 的激动剂的杂环化合物,申请日从2021年至2024年,权利要求涉及化合物通式、具体化合物、中间体和治疗用途等,可见其持续在针对化合物的结构进行优化设计。其中,专利家族PCT/US2021/070507由 Amgen 和 Vigil 共同递交,目前已经有三个US专利获得授权,均保护化合物的具体结构式。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
