随着自体CAR-T疗法的陆续获批,细胞治疗在血液肿瘤领域已取得显著进展。然而,传统ex vivo CAR-T模式仍依赖体外细胞分离、基因改造与扩增流程,整体存在制造周期长、成本较高以及患者可及性受限等问题。在此背景下,in vivo CAR-T作为一种直接在患者体内诱导生成CAR-T细胞的技术,其可以绕开复杂的体外制备流程,更接近形成“通用型制剂”产品,因而具有缩短治疗周期、降低生产成本并提升患者可及性的潜在优势,成为行业关注的前沿方向。
目前,已有多家企业围绕该技术路线推进临床转化。例如,Capstan Therapeutics基于LNP递送mRNA的策略,开发了靶向特定免疫细胞的体内CAR平台,其代表性管线CPTX2309已进入早期临床研究阶段;Interius BioTherapeutics 则依托慢病毒载体平台实现体内T细胞转导,推动针对B细胞相关疾病的候选产品INT2104进入临床阶段。这些研究进展同样验证了体内递送策略在构建CAR-T细胞方面的可行性。
围绕 in vivo CAR-T 的并购与交易活动亦显著升温。Bristol Myers Squibb 以约15亿美元收购 Orbital Therapeutics、AbbVie 以约21亿美元收购 Capstan Therapeutics、Gilead Sciences 以约3.5亿美元收购Interius BioTherapeutics以及AstraZeneca以约10亿美元收购EsoBiotec。近期,Eli Lilly and Company更是以约最高70亿美元的总对价,收购早期临床阶段公司Kelonia Therapeutics。在整体尚处于早期临床阶段的背景下,上述交易规模与节奏反映了头部药企对该技术的前瞻性布局及其潜在产业价值的判断。
整体来看,这些创新药企的主要都在解决同一核心问题,即如何将编码CAR的有效载荷高效且特异性地递送至体内免疫细胞,从而实现功能性表达。
在现有技术框架下,体内递送方式主要集中于两类体系:一类为以慢病毒为代表的病毒载体,依托其天然感染机制实现转导;另一类为以脂质纳米颗粒(LNP)为代表的非病毒递送体系,通过递送mRNA介导表达。
病毒载体
病毒载体是in vivo CAR-T中较早被验证的体内递送体系,通常基于工程化慢病毒或γ-逆转录病毒构建。其结构上主要包括:
经改造的病毒包膜,通过引入细胞特异性结合分子实现靶向性递送,并结合假型化处理的融合元件(fusogen)促进有效载荷进入胞质;以及
病毒内部的表达载荷,通常为包含CAR表达开放阅读框(ORF)的转基因,整体上与传统ex vivo CAR-T体系相似。
在作用机制上,病毒颗粒与T细胞结合后,可通过膜融合或内吞途径进入细胞,随后其RNA在细胞质中经逆转录形成DNA,并被转运至细胞核整合入宿主基因组,从而实现稳定的基因改造;继而CAR转基因被转录为mRNA并在胞质中翻译生成CAR蛋白。
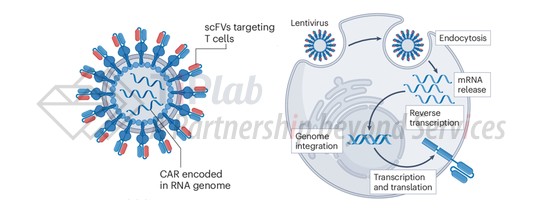
(改编自doi.org/10.1038/s41577-025-01174-1)
LNP载体
LNP载体是in vivo CAR-T中具有代表性的非病毒递送体系,通常由可电离脂质、PEG修饰脂质、辅助磷脂及胆固醇等组成,整体呈“脂质基质包裹RNA载荷”的结构框架,并可通过表面修饰实现功能扩展。
- 在递送层面,既可依赖脂质本身的组织或细胞趋向性实现被动分布,也可通过偶联抗体或其衍生结合分子,实现对特定免疫细胞的主动靶向。
- 其有效载荷主要为RNA形式,包括经UTR优化、密码子优化及核苷修饰的线性mRNA以及通过减少翻译终止、延长表达持续性的环状RNA。
在作用机制上,LNP经细胞内吞后,释放mRNA至胞质,mRNA由核糖体翻译生成CAR分子,从而在体内短暂诱导具有功能的CAR-T细胞。
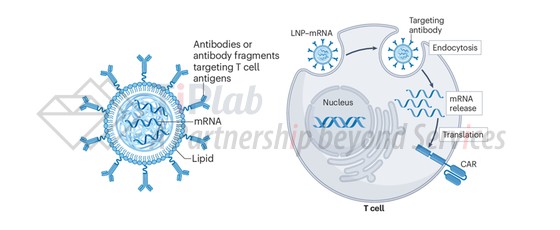
(改编自doi.org/10.1038/s41577-025-01174-1))
总体来看,in vivo CAR-T已由早期概念验证逐步迈入临床探索阶段。围绕“如何将编码CAR的载荷高效且特异性递送至体内免疫细胞”这一核心问题,领域内已涌现出多类关键创新点,不同早期参与者亦围绕这些创新点开展了系统性的专利布局。在此背景下,既有专利保护策略如何为拟进入该领域的玩家提供规划专利布局的思路?同时,考虑不同载体类型的专利布局特点,基于现有技术开展改进的玩家,又有哪些需要重点评估的潜在侵权风险与自由实施空间?在本系列文章中,我们将围绕病毒载体与LNP载体两类体系,与大家分享我们在技术创新点和专利策略中的相关研究。
* 以上文字仅为促进讨论与交流,不构成法律意见或咨询建议。
